
Tại sao thuốc điều trị ung thư tác dụng không đều với các bệnh nhân?
Một nghiên cứu đột phá hé lộ rào cản vật lý bất ngờ khiến các liệu pháp điều trị ung thư hiện đại thất bại: Thuốc bị "mắc kẹt" bên trong các bộ phận nhỏ của tế bào, dẫn đến tình trạng nơi thì quá nồng đặc, nơi lại hoàn toàn trống rỗng.
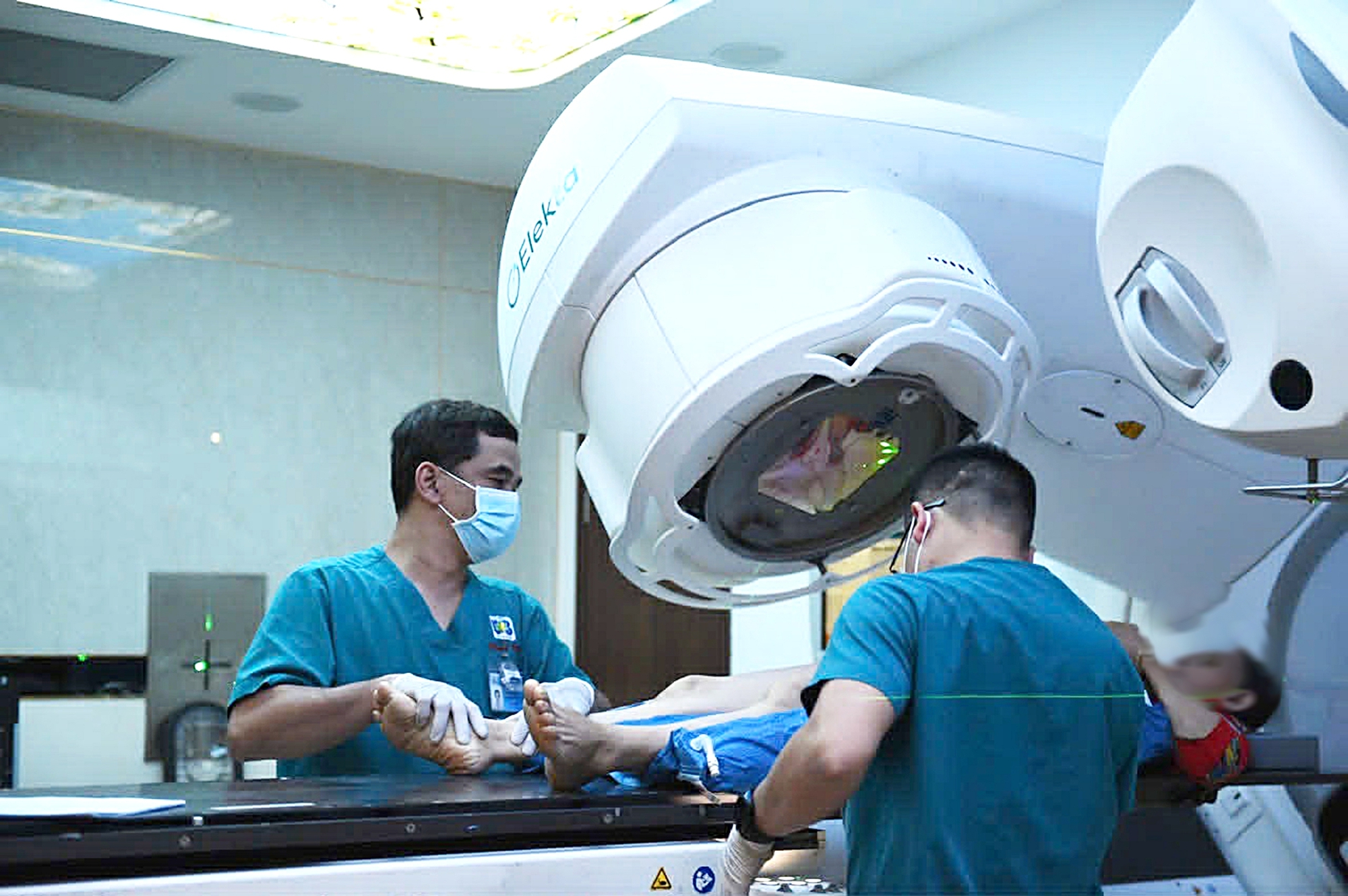
Chuyên viên kỹ thuật xạ trị bệnh nhân ung thư tại Bệnh viện Ung bướu cơ sở 2 (TP.HCM) - Ảnh: TỰ TRUNG
Trong cuộc chiến chống lại ung thư, y học hiện đại đã đạt được những bước tiến khổng lồ với các loại thuốc nhắm mục tiêu (targeted therapy). Tuy nhiên một thực tế nghiệt ngã vẫn tồn tại: cùng một loại thuốc, cùng một liều lượng, có thể cứu sống người này nhưng lại hoàn toàn "bất lực" trước khối u của người khác.
Suốt nhiều thập kỷ, các bác sĩ đã đi tìm câu trả lời cho sự phân hóa sinh tử này. Phải chăng do gene, do cơ địa, hay do khối u đã học được cách "tàng hình"?
Một nghiên cứu vừa được công bố trên tạp chí Nature Communications vào tháng 3-2026 bởi các nhà khoa học thuộc Phòng thí nghiệm Khoa học y tế đã tìm ra một "thủ phạm" nằm ngay bên trong tế bào ung thư. Đó không phải là một siêu năng lực sinh học phức tạp, mà là một cơ chế vật lý đơn giản nhưng đầy tinh vi: Thuốc bị mắc kẹt.
Những "kho chứa ẩn" bên trong mê cung tế bào
Để hiểu được phát hiện này, chúng ta cần nhìn vào cách một loại thuốc ung thư vận hành. Hãy tưởng tượng khối u là một pháo đài và thuốc là những người lính đặc nhiệm được gửi đến để tiêu diệt trung tâm chỉ huy. Để giành chiến thắng, các "binh sĩ" này phải phân tán đều khắp pháo đài và tấn công vào những điểm yếu nhất định của tế bào.
Tuy nhiên nghiên cứu của tiến sĩ Louise Fets và cộng sự đã chỉ ra rằng trong rất nhiều trường hợp, những người lính này chưa kịp chạm đến mục tiêu đã bị "nhốt" vào các phòng kín bên trong pháo đài. Những phòng kín này chính là lysosome, một cấu trúc nhỏ bé được ví như "trung tâm tái chế" hoặc "nhà máy xử lý rác thải" của tế bào.
Bằng công cụ hình ảnh phổ khối lượng hiện đại nhất, nhóm nghiên cứu đã quan sát cách các loại thuốc ức chế PARP (nhóm thuốc chủ lực điều trị ung thư buồng trứng, vú và tuyến tiền liệt) di chuyển bên trong mô khối u thực sự của bệnh nhân.
Nhiều bệnh nhân ban đầu phản ứng rất tốt với thuốc, nhưng chỉ một thời gian sau khối u bùng phát trở lại và không còn chịu tác động của liệu pháp cũ - Ảnh: AI
Khi "nhà máy tái chế" trở thành "chiếc bẫy" giải phóng chậm
Lysosome vốn có nhiệm vụ phân hủy các chất thải và làm sạch tế bào. Thế nhưng đối với một số loại thuốc như niraparib hay rucaparib, lysosome lại giống như một thỏi nam châm cực mạnh, chúng hút các phân tử thuốc vào bên trong và giữ chặt chúng ở đó.
Điều này tạo ra một hệ lụy kép đầy nguy hiểm. Thứ nhất, vì thuốc bị nhốt trong lysosome, nồng độ thuốc tự do trong tế bào không đủ cao để kích hoạt quá trình tiêu diệt tế bào ung thư. Thứ hai, những lysosome này vô tình trở thành các kho chứa giải phóng chậm. Chúng giữ thuốc và nhả ra từng chút một theo thời gian.
Sự phân phối nhỏ giọt này chính là cơ hội vàng để các tế bào ung thư còn sót lại học cách thích nghi. Thay vì bị tiêu diệt ngay, chúng được "luyện tập" với liều lượng thấp, từ đó phát triển cơ chế kháng thuốc mạnh mẽ hơn. Đây chính là lý do tại sao nhiều bệnh nhân ban đầu phản ứng rất tốt với thuốc, nhưng chỉ một thời gian sau khối u bùng phát trở lại và không còn chịu tác động của liệu pháp cũ.
Sự khác biệt giữa các loại thuốc: Không phải mọi "binh sĩ" đều mắc bẫy
Một phát hiện thú vị khác của nhóm nghiên cứu là không phải tất cả các loại thuốc cùng nhóm đều chịu chung số phận. Trong khi niraparib và rucaparib dễ dàng bị lysosome "bắt giữ", thì một loại thuốc tương tự là olaparib lại tỏ ra "thông minh" hơn. Nó không bị thu hút bởi các kho chứa này, mà phân tán đồng đều hơn trong mô khối u.
Phát hiện này có ý nghĩa cực kỳ quan trọng đối với thực hành lâm sàng. Nó giải thích tại sao một bệnh nhân thất bại với loại thuốc này nhưng lại có thể thành công với một loại thuốc khác cùng nhóm. Điều then chốt không chỉ là tên loại thuốc, mà là cấu trúc phân tử của nó có "hấp dẫn" đối với các lysosome trong tế bào của bệnh nhân đó hay không.
Sử dụng phương pháp giải trình tự không gian kết hợp với chụp ảnh phổ khối lượng, các nhà khoa học đã có thể tạo ra các bản đồ chi tiết cho thấy sự tương tác giữa gene và nồng độ thuốc. Họ phát hiện ra rằng ngay cả trong cùng một khối u của một người, các khu vực khác nhau có biểu hiện gene khác nhau, dẫn đến khả năng hấp thụ thuốc khác nhau.
Tiến sĩ Zoe Hall, phó giáo sư tại Imperial College London, nhấn mạnh: "Thông qua việc lập bản đồ không gian của các phân tử thuốc, chúng tôi có thể xác định chính xác các vùng có nồng độ thuốc cao và thấp. Điều này cho phép chúng tôi hiểu tại sao thuốc lại hiệu quả với khu vực này mà không hiệu quả với khu vực kia".
Những thách thức phía trước và niềm hy vọng mới
Dù nghiên cứu trên các "mẫu cấy ghép" sống đã mang lại những kết quả chấn động, các nhà khoa học vẫn thừa nhận rằng cơ thể con người thực tế phức tạp hơn nhiều. Trong một cơ thể sống, thuốc phải di chuyển qua hệ thống mạch máu thường bị rối loạn bên trong khối u trước khi tiếp cận được tế bào.
Trong giai đoạn tiếp theo, nhóm nghiên cứu dự định mở rộng thí nghiệm trên các mô hình động vật và các nhóm bệnh nhân lớn hơn. Họ muốn hiểu rõ hơn về "dấu ấn phân tử", những đặc điểm di truyền cụ thể khiến một người có nhiều hoặc ít các kho chứa thuốc lysosome.
"Chúng ta đang tiến gần hơn bao giờ hết đến mục tiêu điều trị cá nhân hóa hoàn toàn", tiến sĩ Louise Fets chia sẻ. "Hiểu được cách tế bào 'nhốt' thuốc chính là chìa khóa để chúng ta mở cánh cửa bế tắc trong việc kháng thuốc và tái phát ung thư".
Link nội dung: https://phapluatcongdan.vn/tai-sao-thuoc-dieu-tri-ung-thu-tac-dung-khong-deu-voi-cac-benh-nhan-a46510.html